BLACK FRIDAY
Celebrating 25 years Est 1999-2024
Save up to 60%* for Level 2 Lite
1 year 40%, 2 years 50% and *3 years 60%
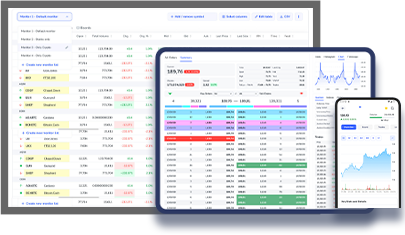
Real-time Prices | Level 2 | |
|---|---|---|
London Stock Exchange | ||
Chi-X Europe | ||
BATS Europe | ||
Aquis Exchange | ||
New York Stock Exchange | ||
NASDAQ | ||
American Stock Exchange | ||
Dow Jones Indices | ||
Precious Metal |

*Across 3 years £2132.64 only £853.06